З наукової точки зору довжина хвилі у видимому діапазоні – це основні компоненти сонячного світла, які пройшли через земну атмосферу. Їх особливість ґрунтується виключно на здатності людської сітківки ока реагувати на них і значною мірою їх розрізняти, що і є основою поняття кольору.
Наприклад, біле світло (звичайне денне світло) – це суміш всіх довжин хвиль у діапазоні 380-760 нм, на які реагує людське око, а також інфрачервоного та ультрафіолетового променів, які не сприймаються людським оком. Коли об’єкт поглинає частину випромінювання цього діапазону, то сприймаються хвилі, що залишилися, і об’єкт виглядає кольоровим. Наприклад, якщо червоні промені видалити з білого світла, людина бачитиме синьо-зелений колір. Синьо-зелений доповнює червоний, а червоний доповнює синьо-зелений. Такі кольори називають додатковими (див. табл. 1).
Таблиця 1. Поглинання світла, що залишає додатковий колір
| Видалено | Спостерігається |
|---|---|
| Фіалковий | Жовто-зелений |
| Синій | Жовтий |
| Блакитний | Помаранчевий |
| Синьо-зелений | Червоний |
| Зелений | Фіолетовий |
| Жовто-зелений | Фіалковий |
| Жовтий | Синій |
| Помаранчевий | Блакитний |
| Червоний | Синьо-зелений |
| Фіолетовий | Зелений |
Коли об’єкт відбиває майже всі промені світла, людина бачить білий колір. Коли не відбивається жоден промінь – чорний. Якщо подивитися на веселку, ви не побачите чорного кольору у видимому спектрі кольорів. Усі кольори є відбиттям світла, крім чорного. Чорний – це відсутність світла. На відміну від білих та інших об’єктивне є помилковим. З цієї причини необхідно посилатися на довжини хвиль, які використовуються, а не описувати реакцію людини на них. Тому сприйняття кольору є лише еволюційним пристосуванням людини до відсутності деяких довжин хвиль у білому світлі.
Барвниками називають інтенсивно забарвлені речовини, які придатні для фарбування різноманітних матеріалів (тканини, папір, поліграфічні та фотоматеріали, лікарські засоби, полімерні матеріали тощо). Колір як природних, так штучних (синтетичних) барвників пов'язаний із вибірковістю поглинати частину хвиль видимого спектра , відбиваючи решту хвиль. До того ж колір барвників залежить від їх хімічного складу – наявності ланцюгів спряження (чергування простих та подвійних зв'язків) і ароматичних або гетероциклічних ядер відтінків, чистий чорний колір може існувати в природі без будь-якого світла взагалі.
Слід розуміти, що вони є індивідуальними хімічними речовинами, і, як і всі сполуки вони можуть мати подібні до певних речовин хімічні реакції, а також вступати у специфічні.
Барвники у своїй більшості мають бензенове кільце, і як відомо бензен є безбарвною рідиною. Насправді ж він поглинає електромагнітне випромінювання так само, як і барвники, але робить це приблизно при довжині хвилі 200 нм, тому ця сполука не помітна людському оку.
Оскільки, за визначенням, барвники є ароматичними сполуками, їх структура включає ароматичне кільце, яке має делокалізовані електронні системи. Вони відповідають за поглинання електромагнітного випромінювання різних довжин хвиль залежно від енергії електронних хмар. З цієї причини хромофори не забарвлюють барвники в тому сенсі, що вони надають їм здатність поглинати випромінювання. Швидше, хромофори функціонують, змінюючи енергію в делокалізованій електронній хмарі барвника, і ця зміна призводить до того, що сполука поглинає випромінювання з видимого діапазону, а не за його межами.
Хромофори – це атомні конфігурації, які можуть змінювати енергію в делокалізованих системах. Вони складаються з атомів, з’єднаних послідовно, сполученими одинарними і подвійними зв’язками, що чергуються (тобто спряженими, див. рис. 1).
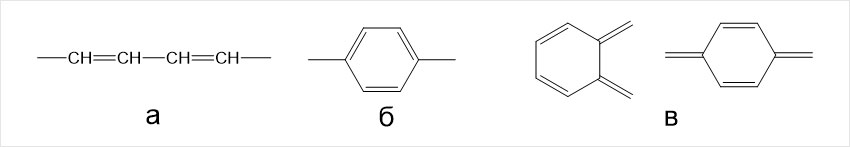
Рис. 1. Хромофорні групи:
а – спряжені подвійні зв’язки; б – бензенове кільце; в – орто- та парахіноїдні кільцеві хромофори
Хромофорні конфігурації часто існують у вигляді кількох одиниць, які мають кон’юговані подвійні зв’язки, і є більш ефективними. Це пов’язано з взаємодією між подвійними зв’язками, яка спричиняє часткову делокалізацію електронів, що беруть участь в утворенні зв’язків. У цьому випадку, хоча у зв’язках беруть участь певні атоми, електрони розподіляються на більшій площі, ніж конкретні атоми, а також залучають сусідні атоми, які мають подвійні зв’язки.
В ультрафіолетовій та видимій областях (між 200 і 800 нм) поглинання фотонів зумовлено їх взаємодією з зовнішньою оболонкою молекул (з валентними електронами). Збуджені фотонами електрони можуть переходити з одного стаціонарного стану в інший. Ці переходи можуть бути зв'язаними і незв'язаними з випромінюванням. У першому випадку молекулярна система випромінює або поглинає електромагнітні випромінювання. Деякі речовини в результаті поглинання фотонів люмінесціюють. В інших речовинах поглинання фотонів викликає теплові та хімічні явища. Відомо, що поглинання видимого й ультрафіолетового світла може викликати порушення хімічних зв'язків і сприяти виникненню хімічних реакцій.
Контроль кольору або контроль відтінку розчинів барвників є поширеним завданням для галузей промисловості, що мають справу з барвниками, а саме текстильної промисловості, виробництва фарби, друкарської галузі тощо. Велика різноманітність відтінків регулярно відтворюється сумішшю барвників у лакофарбовій промисловості. Однією з найважливіших проблем у цьому процесі є визначення точних пропорцій барвників, для забезпечення відповідності кольору цільовому відтінку. Для кількісного аналізу розчинів барвників можна використовувати різноманітні аналітичні методи, однак серед усіх абсорбційних найпоширенішим залишається спектроскопія УФ-видимого діапазону.
Основним принципом кількісної УФ-видимої спектрофотометрії є лінійна залежність між поглинанням і концентрацією розчиненого зразка, прозорої рідини або твердої речовини, яка визначається законом Бера-Ламберта (див. рис. 2).
![]()
Рис. 2. Формула закона Ламберта-Бера:
A – поглинання на певній довжині хвилі (зазвичай максимум λmax),
a – питомий коефіцієнт поглинання або екстинкції,
l – довжина шляху, C – концентрація барвника.
Усі багатокомпонентні кількісні методи базуються на принципі, згідно з яким поглинання суміші на будь-якій довжині хвилі дорівнює сумі поглинання кожного компонента в суміші на цій довжині хвилі.
Простий підхід до багатокомпонентного аналізу базується на вимірюваннях на довжинах хвиль, які дорівнюють кількості компонентів у суміші. Зазвичай вибираються довжини хвиль, що відповідають максимуму поглинання кожного компонента. Для калібрування вимірюється абсорбція стандартів із відомими концентраціями чистих компонентів, щоб визначити коефіцієнт екстинкції для кожного компонента на кожній вибраній довжині хвилі. Таким чином, для двох компонентів із концентраціями C1 і C2 рівняння мають вигляд (див. рис. 3):
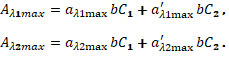
Рис. 3. Рівняння для кількісного розрахунку концентрації компонентів барвника:
α та α' – коефіцієнти поглинання барвників,
C – концентрація, b – довжина шляху.
У випадку бінарних сумішей, наприклад, червоний-рубіновий, через спектральне перекривання спектрів нульового порядку (див. рис. 4), одночасне визначення обох барвників не є точним за методом прямих вимірювань поглинання. Деякі можливості, які можуть бути обрані для вирішення цієї проблеми, це похідні спектрофотометричні методи, такі як перетин через нуль або методи похідних спектрів співвідношення.

Рис. 4. Спектри поглинання барвників: 0,025 г/л рубінового, 0,025 г/л червоного та їх бінарної суміші
Для визначення вмісту барвника у зразках, приготованих із використанням бінарних сумішей барвників, застосовують також математичні моделі, що полягають у отриманні похідних від спектрів співвідношення поглинання по довжині хвилі. На практиці спектр співвідношення можна отримати, поділивши спектр поглинання бінарної суміші двох барвників на стандартний спектр поглинання одного з компонентів. Калібрувальні графіки можна підготувати, побудувавши значення похідної співвідношення відносно їхніх відповідних концентрацій.
Незважаючи на регламентоване застосування барвників в різних галузях промисловості (особливо у харчовій або фармацевтичній продукції) спостерігаються випадки їх безконтрольного використання із перевищенням допустимих концентрацій і фальсифікації продуктів. Суворі правила щодо використання особливо синтетичних барвників спрямовані на захист здоров'я населення та забезпечення безпеки споживачів, особливо дітей, і часто пов'язані із ретельним тестуванням та оцінкою натуральних кольорів перед їх затвердженням. Дана ситуація призвела до необхідності розроблення сучасних і оперативних методів їх якісного і кількісного контролю, що є непростим завданням.
Серед широкого спектру аналітичних методів, таких як різноманітні спектрофотометричні методи, тонкошарова хроматографія, високоефективна рідинна хроматографія, розроблення методик аналізу барвників на основі ультрафіолетової (УФ) спектроскопії залишається затребуваним завдяки доступності обладнання і диференційованого вибору визначення залежно від складу барвників.
Г.Г. Жалніна, доцент, кандидат хімічних наук, кафедра хімії Національного університету «Києво-Могилянська академія»








![Математика: проблеми теорії чисел [2]](/images/202404ua/numbers-theory.jpg)






![Теоретична фізика: яка вона [2]](/images/202504ua/theoretical-physics.jpg#joomlaImage://local-images/202504ua/theoretical-physics.jpg?width=850&height=587)
 Засновник та видавець
Засновник та видавець